Wiązka zadań
Czy wszystkie tlenki reagują z kwasami?
Zadanie
Do probówki z roztworem kwasu solnego dodano jako wskaźnik oranż metylowy, który zabarwił się na czerwono. Roztwór rozlano do trzech probówek, do których następnie wsypano trzy różne tlenki: tlenek sodu, tlenek fosforu(III) i tlenek krzemu(IV). Przebieg doświadczenia przedstawiono na rysunku:
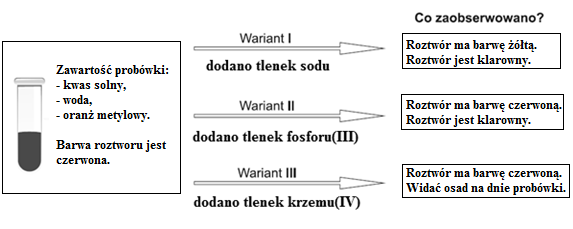
Na podstawie obserwacji z doświadczenia określ, które z tlenków reagują z kwasem solnym:
| Czy reaguje z kwasem solnym? | TAK czy NIE? | |
| 1. | tlenek sodu | `square` TAK / `square` NIE |
| 2. | tlenek fosforu(III) | `square` TAK / `square` NIE |
| 3. | tlenek krzemu(IV) | `square` TAK / `square` NIE |
Poprawna odpowiedź
1. TAK, 2. NIE, 3. NIE.
Wymaganie ogólne
1 Pozyskiwanie, przetwarzanie i tworzenie informacji. Uczeń korzysta z chemicznych tekstów źródłowych, pozyskuje, analizuje, ocenia i przetwarza informacje pochodzące z różnych źródeł, ze szczególnym uwzględnieniem mediów i Internetu.
Wymaganie szczegółowe
3.1 Reakcje chemiczne. Uczeń opisuje różnice w przebiegu zjawiska fizycznego i reakcji chemicznej / podaje przy kłady zjawisk fizycznych i reakcji chemicznych zachodzących w otoczeniu człowieka/ planuje i wykonuje doświadczenia ilustrujące zjawisko fizyczne i reakcję chemiczną.
3.2 Reakcje chemiczne. Uczeń opisuje, na czym polega reakcja syntezy, analizy i wymiany/ podaje przykłady różnych typów reakcji i zapisuje odpowiednie równania/ wskazuje substraty i produkty/ dobiera współczynniki w równaniach reakcji chemicznych/ obserwuje doświadczenia ilustrujące typy reakcji i formułuje wnioski.
7.4 Sole. Uczeń pisze równania reakcji otrzymywania soli (reakcje: kwas + wodorotlenek metalu, kwas + tlenek metalu, kwas + metal, wodorotlenek metalu + tlenek niemetalu).
Komentarz
Prezentowane zadanie proponujemy na lekcję przed egzaminem gimnazjalnym, szczególnie w tych klasach, w których uczniowie nie wykonują na lekcjach samodzielnie doświadczeń chemicznych. Porusza ono problem sprawdzania bardzo ważnej umiejętności w chemii – wnioskowania na podstawie objawów reakcji. Uwrażliwianie uczniów na to co mogą zaobserwować, a więc na: zmiany barwy i postaci substancji, ich zapach, efekty cieplne i akustyczne reakcji powinno stanowić ważny element każdych zajęć eksperymentalnych. Przedstawiony w zadaniu układ doświadczalny nie pochodzi wprost z zestawu zalecanych doświadczeń wymienionych w komentarzu do podstawy programowej przedmiotu chemia, więc uczeń najprawdopodobniej po raz pierwszy będzie analizował jego przebieg. Pozwala to na ocenę faktycznych umiejętności nabytych przez ucznia dotyczących analizy przebiegu doświadczenia oraz wyciągania wniosków na podstawie obserwacji bez odwoływania się do wiedzy encyklopedycznej. Komentarz do podstawy programowej przedmiotu chemia dla III etapu edukacyjnego definiuje bowiem pojęcie wnioskowania w następujący sposób: „(od ucznia) nie oczekujemy odpowiedzi na podstawie zapamiętanych wiadomości, ma ona być wynikiem zauważenia logicznego związku pomiędzy różnymi fragmentami informacji (przedstawionej w różnej formie, również, jako obserwowane przez ucznia zjawisko)”..
Schemat doświadczenia poprzedzony krótkim wstępem przedstawia opis zawartości probówek przed i po doświadczeniu. Obserwacje te odnoszą się do barwy roztworu oraz jego klarowności. Analizując schemat doświadczenia, uczeń powinien zauważyć, że:
- badany układ składa się tak naprawdę z trzech próbówek,
- we wszystkich probówkach na początku doświadczenia jest roztwór kwasu solnego i oranż metylowy,
- wszystkie trzy użyte w doświadczeniu tlenki mają stan skupienia stały.
Aby poprawnie odpowiedzieć na pytanie, uczeń powinien ponadto wiedzieć, że roztwór oranżu metylowego w kwasie jest klarowny, jak również to, że zmiana barwy oraz pojawienie się lub zniknięcie osadu może być objawem reakcji chemicznej.
Wnioskowanie zazwyczaj składa się z kilku etapów, w zależności od postawionej hipotezy. Pierwszym etapem jest najczęściej określenie, czy w badanym układzie w ogóle zaszła reakcja chemiczna. Przedstawione zadanie dotyczy sprawdzania właśnie tej umiejętności. Aby poprawnie odpowiedzieć na pytanie, uczeń powinien wywnioskować, że:
- w probówce pierwszej zaszła reakcja, ponieważ oranż metylowy zmienił barwę oraz roztwór jest klarowny mimo to, że wsypano do niego tlenek, czyli – tlenek sodu reaguje z kwasem solnym,
- w próbówce drugiej nie zaszła reakcja między tlenkiem fosforu(III) a kwasem, roztwór jest nadal klarowny, a oranż metylowy ma dalej czerwoną barwę, a więc – tlenek fosforu(III) nie reaguje z kwasem solnym,
- w trzeciej probówce nie zaszła reakcja (tlenek opadł na dno probówki, oranż nie zmienił barwy), czyli – tlenek krzemu(IV) nie reaguje z kwasem solnym.
Nauczyciel może wyjaśnić uczniom, że w próbówce drugiej zachodzi reakcja między tlenkiem fosforu(III) a wodą, w wyniku której powstaje kwas.
W celu dokładnego przeanalizowania układu eksperymentalnego przedstawionego w zadaniu, warto, aby przed jego rozwiązywaniem nauczyciel przedyskutował z uczniami następujące problemy:
- Co oznacza zmiana barwy wskaźnika w roztworze?
- Co oznacza brak zmiany barwy wskaźnika w roztworze?
- Jakie objawy towarzyszą rozpuszczaniu, a jakie roztwarzaniu substancji?
- W jakiej sytuacji osad, który powstał w próbówce po doświadczeniu, jest objawem reakcji, a w jakiej nie jest?
Przedstawione zadanie, po ewentualnej modyfikacji, może być również inspiracją do przeprowadzenia eksperymentu. Warto wtedy zaproponować uczniom zadanie pytań badawczych oraz przedstawienie hipotez, a następnie ich weryfikację już po przeprowadzeniu czynności doświadczalnych.
Utwór jest chroniony prawem autorskim. Zasady i warunki korzystania z niego określa Regulamin Serwisu Bazy Dobrych Praktyk.
"Masz uwagi do treści? Uważasz, że zawiera błąd? Napisz na bnd@ibe.edu.pl





